生物化学与分子生物学/蛋白质的分子组成
蛋白质的结构与功能-
蛋白质的分子组成 -
蛋白质的分子结构 -
蛋白质结构与功能的关系 -
蛋白质的理化性质
生物体结构越复杂,其蛋白质种类和功能也越繁多。具有复杂空间结构的蛋白质(protein)不仅是生物体的重要结构物质之一,而且承担着各种生物学功能,其动态功能包括化学催化反应、免疫反应、血液凝固、物质代谢调控、基因表达调控和肌收缩等功能;就其结构功能而言,蛋白质提供结缔组织和骨的基质、形成组织形态等。显而易见,普遍存在于生物界的蛋白质是生物体的重要组成成分和生命活动的基本物质基础,也是生物体中含量最丰富的生物大分子(biomacromolecule), 约占人体固体成分的45%,而在细胞中可达细胞干重的70%以上。蛋白质分布广泛,几乎所有的器官组织都含有蛋白质。一个真核细胞可有数万种蛋白质,各自有特殊的结构和功能。
尽管蛋白质的种类繁多,结构各异,但元素组成相似,主要有碳(50%~55%)、氢(6%~7%)、氧(19%~24%)、氮(13%~19%)和硫(0~4%)。有些蛋白质还含有少量磷或金属元素铁、铜、锌、锰、钴、钼等,个别蛋白质还含有碘。
各种蛋白质的含氮量很接近,平均为16%。由于蛋白质是体内的主要含氮物质,因此测定生物样品的含氮量就可按下式推算出蛋白质大致含量:
每克样品含氮克数×6.25×100=100g样品中蛋白质含量(g%)。
L-α-氨基酸是蛋白质的基本结构单位
[编辑]人体内蛋白质是以20种氨基酸(amino acid)为原料合成的多聚体,因此氨基酸是组成蛋白质的基本单位,只是不同蛋白质的各种氨基酸的含量与排列顺序不同。蛋白质受酸、碱或蛋白酶作用而水解产生游离氨基酸。存在于自然界中的氨基酸有300余种,参与蛋白质合成的氨基酸一般有20种,通常是L-α-氨基酸(甘氨酸除外,无D,L之分)。
连在—COO-基上的碳称为α-碳原子,为不对称碳原子(甘氨酸除外),不同的氨基酸其侧链(R)结构各异。
除了20种基本的氨基酸外,近年发现硒代半胱氨酸在某些情况下也可用于合成蛋白质。硒代半胱氨酸从结构上来看,硒原子替代了半胱氨酸分子中的硫原子。硒代半胱氨酸存在于少数天然蛋白质中,包括过氧化物酶和电子传递链中的还原酶等。硒代半胱氨酸参与蛋白质合成时,并不是由目前已知的密码子编码,具体机制尚不完全清楚。另外在产甲烷菌的甲胺甲基转移酶中发现了吡咯赖氨酸。D型氨基酸至今仅发现于微生物膜内的D-谷氨酸、个别抗生素中(例如短杆菌肽含有D-苯丙氨酸)及低等生物体内(例如蚯蚓D-丝氨酸)。
人体内也存在若干不参与蛋白质合成但具有重要生理作用的L-α-氨基酸,如参与合成尿素的鸟氨酸(ornithine)、瓜氨酸(citrulline)和精氨酸代琥珀酸(argininosuccinate)。
氨基酸可根据侧链结构和理化性质进行分类
[编辑]20种氨基酸根据其侧链的结构和理化性质可分成5类:①非极性脂肪族氨基酸;②极性中性氨基酸;③芳香族氨基酸;④酸性氨基酸;⑤碱性氨基酸。
| 结构式 | 中文名 | 英文名 | 缩写 | 符号 | 等电点(pI) |
|---|---|---|---|---|---|
|
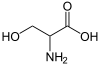
丝氨酸 | Serine | Ser | S | 5.68 |
|
半胱氨酸 | Cysteine | Cys | C | 5.07 |

|
天冬酰胺 | Asparagine | Asn | N | 5.41 |
|
谷氨酰胺 | Glutamine | Gln | Q | 5.65 |

|
苏氨酸 | Threonine | Thr | T | 5.60 |
| 结构式 | 中文名 | 英文名 | 缩写 | 符号 | 等电点(pI) |
|---|---|---|---|---|---|

|
苯丙氨酸 | Phenylalanine | Phe | F | 5.48 |
| 色氨酸 | Tryptophan | Trp | W | 5.89 | |
| 酪氨酸 | Tyrosine | Tyr | Y | 5.66 |
| 结构式 | 中文名 | 英文名 | 缩写 | 符号 | 等电点(pI) |
|---|---|---|---|---|---|

|
天冬氨酸 | Aspartic Acid | Asp | D | 2.97 |
|
谷氨酸 | Glutamic Acid | Glu | E | 3.22 |
| 结构式 | 中文名 | 英文名 | 缩写 | 符号 | 等电点(pI) |
|---|---|---|---|---|---|
|
赖氨酸 | Lysine | Lys | K | 9.74 |
| 精氨酸 | Arginine | Arg | R | 10.76 | |

|
组氨酸 | Histidine | His | H | 7.59 |
一般而言,非极性脂肪族氨基酸在水溶液中的溶解度小于极性中性氨基酸;芳香族氨基酸中苯基的疏水性较强,酚基和吲哚基在一定条件下可解离;酸性氨基酸的侧链都含有羧基;而碱性氨基酸的侧链分别含有氨基、胍基或咪唑基。
脯氨酸和半胱氨酸结构较为特殊。脯氨酸应属亚氨基酸,N在杂环中移动的自由度受限制,但其亚氨基仍能与另一羧基形成肽键。脯氨酸在蛋白质合成加工时可被修饰成经脯氨酸;半胱氨酸巯基失去质子的倾向较其他氨基酸为大,其极性最强;2个半胱氨酸通过脱氢后以二硫键相连接,形成胱氨酸。蛋白质中有不少半胱氨酸以胱氨酸形式存在。
在蛋白质翻译后的修饰过程中,脯氨酸和赖氨酸可分别被羟化为羟脯氨酸和羟赖氨酸。蛋白质分子中20种氨基酸残基的某些基团还可被甲基化、甲酰化、乙酰化、异戊二烯化和磷酸化等。这些翻译后修饰,可改变蛋白质的溶解度、稳定性、亚细胞定位和与其他细胞蛋白质相互作用的性质等,体现了蛋白质生物多样性的一个方面。
氨基酸具有共同或特异的理化性质
[编辑]氨基酸具有两性解离的性质
[编辑]由于所有氨基酸都含有碱性的α-氨基和酸性的α-羧基,可在酸性溶液中与质子(H+)结合呈带正电荷的阳离子 (—NH3+), 也可在碱性溶液中与OH-结合,失去质子变成带负电荷的阴离子(—COO-), 因此氨基酸是一种两性电解质,具有两性解离的特性。氨基酸的解离方式取决于其所处溶液的酸碱度。在某一pH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性,此时溶液的pH称为该氨基酸的等电点(amino acid isoelectric point ,pI)。
通常氨基酸的等电点(pI)是由α-羧基和α-氨基的解离常数的负对数pK1和pK2决定的。
pI的计算公式为:pI=(pK1+pK2)。
如丙氨酸pK-COOH=2.34,pK-NH2=9.69,所以丙氨酸的pI=(2.34+9.69)=6.02。
若一个氨基酸有3个可解离基团,写出它们电离式后取兼性离子两边的pK的平均值,即为此氨基酸的pl。
含共轭双键的氨基酸具有紫外吸收性质
[编辑]根据氨基酸的吸收光谱,含共轭双键的Trp和Tyr的最大吸收峰在280nm波长附近。由于大多数蛋白质含有Trp和Tyr残基,因此测定蛋白质溶液280nm的光吸收值是分析溶液中蛋白质含量的快速简便的方法。
氨基酸与茚三酮反应生成蓝紫色化合物
[编辑]茚三酮反应(ninhydrin reaction)指的是茚三酮水合物在弱酸性溶液中与氨基酸共加热时,氨基酸被氧化脱氨、脱羧,而茚三酮水合物被还原,其还原物可与氨基酸加热分解产生的氨结合,再与另一分子茚三酮缩合成为蓝紫色的化合物,此化合物最大吸收峰在570nm波长处。由于此吸收峰值的大小与氨基酸释放出的氨量成正比,因此可作为氨基酸定量分析方法。
氨基酸通过肽链连接而形成蛋白质或肽
[编辑]蛋白质中的氨基酸相互结合而生成肽(peptide), 例如1分子甘氨酸的α-羧基和1分子甘氨酸的α-氨基脱去1分子水缩合成为甘氨酰甘氨酸,这是最简单的肽,即二肽。α-羧基和α-氨基脱水形成酰胺键,称为肽键。二肽通过肽键与另一分子氨基酸缩合生成三肽。此反应可继续进行,依次生成四肽、五肽......
一般而言,由2~20个氨基酸相连而成的肽称为寡肽(oligopeptide), 而更多的氨基酸相连而成的肽称为多肽(polypeptide)。多肽链有两端,其游离α-氨基的一端称氨基末端(amino terminal)或N-端,游离α-羧基的一端称为羧基末端(carboxyl terminal)或C-端。肽链中的氨基酸分子因脱水缩合而基团不全,被称为氨基酸残基(amino acid residue)。
蛋白质是由许多氨基酸残基组成、折叠成特定的空间结构、并具有特定生物学功能的多肽。一般而论,蛋白质的氨基酸残基数通常在50个以上,50个氨基酸残基以下则仍称为多肽。例如,常把由39个氨基酸残基组成的促肾上腺皮质激素称作为多肽,而把含有51个氨基酸残基、分子量为 5733的胰岛素称作蛋白质。
生物活性肽具有生理活性及多样性
[编辑]人体内存在许多具有生物活性的低分子量的肽,有的仅三肽,有的属寡肽或多肽,在代谢调节、神经传导等方面起着重要的作用。随着肽类药物的发展,许多化学合成或重组DNA技术制备的肽类药物和疫苗已在疾病预防和治疗方面取得成效。
谷胱甘肽(GSH)
[编辑]
谷胱甘肽(glutathione, GSH)是由谷氨酸、半胱氨酸和甘氨酸组成的三肽。第一个肽键是非α肽键,由谷氨酸γ-羧基与半胱氨酸的氨基组成, 分子中半胱氨酸的巯基是该化合物的主要功能基团。
GSH的巯基具有还原性,可作为体内重要的还原剂保护蛋白质或酶分子中的巯基免遭氧化,使蛋白质或酶处在活性状态。在谷胱甘肽过氧化物酶的催化下,GSH可还原细胞内产生的H2O2, 使其变成H2O, 与此同时,GSH被氧化成氧化型谷胱甘肽(GSSG), 后者在谷胱甘肽还原酶催化下,再生成GSH。
此外,GSH的巯基还有嗜核特性,能与外源的嗜电子毒物如致癌剂或药物等结合,从而阻断这些化合物与DNA、RNA或蛋白质结合,以保护机体免遭毒物损害。
多肽类激素及神经肽体
[编辑]内有许多激素属寡肽或多肽,例如属于下丘脑-垂体-肾上腺皮质轴的催产素(9肽)、加压素(9肽)、促肾上腺皮质激素(39肽)、促甲状腺素释放激素(3肽)等。
促甲状腺素释放激素是一个特殊结构的三肽, 其N-端的谷氨酸环化成为焦谷氨酸(pyroglutamjc acid),C-端的脯氨酸残基酰化成为脯氨酰胺,它由下丘脑分泌,可促进腺垂体分泌促甲状腺素。
有一类在神经传导过程中起信号转导作用的肽类被称为神经肽(neuro peptide)。较早发现的有脑啡肽(5肽)、β-内啡肽(31肽)和强啡肽(17肽)等。近年还发现孤啡肽(17肽),其一级结构类似于强啡肽。它们与中枢神经系统产生痛觉抑制有密切关系。因此很早就被用于临床的镇痛治疗。除此以外,神经肽还包括P物质(10肽)、神经肽Y等。