生物化學與分子生物學/蛋白質的分子組成
蛋白質的結構與功能-
蛋白質的分子組成 -
蛋白質的分子結構 -
蛋白質結構與功能的關係 -
蛋白質的理化性質
生物體結構越複雜,其蛋白質種類和功能也越繁多。具有複雜空間結構的蛋白質(protein)不僅是生物體的重要結構物質之一,而且承擔著各種生物學功能,其動態功能包括化學催化反應、免疫反應、血液凝固、物質代謝調控、基因表達調控和肌收縮等功能;就其結構功能而言,蛋白質提供結締組織和骨的基質、形成組織形態等。顯而易見,普遍存在於生物界的蛋白質是生物體的重要組成成分和生命活動的基本物質基礎,也是生物體中含量最豐富的生物大分子(biomacromolecule), 約占人體固體成分的45%,而在細胞中可達細胞乾重的70%以上。蛋白質分布廣泛,幾乎所有的器官組織都含有蛋白質。一個真核細胞可有數萬種蛋白質,各自有特殊的結構和功能。
儘管蛋白質的種類繁多,結構各異,但元素組成相似,主要有碳(50%~55%)、氫(6%~7%)、氧(19%~24%)、氮(13%~19%)和硫(0~4%)。有些蛋白質還含有少量磷或金屬元素鐵、銅、鋅、錳、鈷、鉬等,個別蛋白質還含有碘。
各種蛋白質的含氮量很接近,平均為16%。由於蛋白質是體內的主要含氮物質,因此測定生物樣品的含氮量就可按下式推算出蛋白質大致含量:
每克樣品含氮克數×6.25×100=100g樣品中蛋白質含量(g%)。
L-α-胺基酸是蛋白質的基本結構單位
[編輯]人體內蛋白質是以20種胺基酸(amino acid)為原料合成的多聚體,因此胺基酸是組成蛋白質的基本單位,只是不同蛋白質的各種胺基酸的含量與排列順序不同。蛋白質受酸、鹼或蛋白酶作用而水解產生游離胺基酸。存在於自然界中的胺基酸有300餘種,參與蛋白質合成的胺基酸一般有20種,通常是L-α-胺基酸(甘氨酸除外,無D,L之分)。
連在—COO-基上的碳稱為α-碳原子,為不對稱碳原子(甘氨酸除外),不同的胺基酸其側鏈(R)結構各異。
除了20種基本的胺基酸外,近年發現硒代半胱氨酸在某些情況下也可用於合成蛋白質。硒代半胱氨酸從結構上來看,硒原子替代了半胱氨酸分子中的硫原子。硒代半胱氨酸存在於少數天然蛋白質中,包括過氧化物酶和電子傳遞鏈中的還原酶等。硒代半胱氨酸參與蛋白質合成時,並不是由目前已知的密碼子編碼,具體機制尚不完全清楚。另外在產甲烷菌的甲胺甲基轉移酶中發現了吡咯賴氨酸。D型胺基酸至今僅發現於微生物膜內的D-穀氨酸、個別抗生素中(例如短桿菌肽含有D-苯丙氨酸)及低等生物體內(例如蚯蚓D-絲氨酸)。
人體內也存在若干不參與蛋白質合成但具有重要生理作用的L-α-胺基酸,如參與合成尿素的鳥氨酸(ornithine)、瓜氨酸(citrulline)和精氨酸代琥珀酸(argininosuccinate)。
胺基酸可根據側鏈結構和理化性質進行分類
[編輯]20種胺基酸根據其側鏈的結構和理化性質可分成5類:①非極性脂肪族胺基酸;②極性中性胺基酸;③芳香族胺基酸;④酸性胺基酸;⑤鹼性胺基酸。
| 結構式 | 中文名 | 英文名 | 縮寫 | 符號 | 等電點(pI) |
|---|---|---|---|---|---|
|
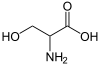
絲氨酸 | Serine | Ser | S | 5.68 |
|
半胱氨酸 | Cysteine | Cys | C | 5.07 |

|
天冬醯胺 | Asparagine | Asn | N | 5.41 |
|
穀氨醯胺 | Glutamine | Gln | Q | 5.65 |

|
蘇氨酸 | Threonine | Thr | T | 5.60 |
| 結構式 | 中文名 | 英文名 | 縮寫 | 符號 | 等電點(pI) |
|---|---|---|---|---|---|

|
苯丙氨酸 | Phenylalanine | Phe | F | 5.48 |
| 色氨酸 | Tryptophan | Trp | W | 5.89 | |
| 酪氨酸 | Tyrosine | Tyr | Y | 5.66 |
| 結構式 | 中文名 | 英文名 | 縮寫 | 符號 | 等電點(pI) |
|---|---|---|---|---|---|

|
天冬氨酸 | Aspartic Acid | Asp | D | 2.97 |
|
穀氨酸 | Glutamic Acid | Glu | E | 3.22 |
| 結構式 | 中文名 | 英文名 | 縮寫 | 符號 | 等電點(pI) |
|---|---|---|---|---|---|
|
賴氨酸 | Lysine | Lys | K | 9.74 |
| 精氨酸 | Arginine | Arg | R | 10.76 | |

|
組氨酸 | Histidine | His | H | 7.59 |
一般而言,非極性脂肪族胺基酸在水溶液中的溶解度小於極性中性胺基酸;芳香族胺基酸中苯基的疏水性較強,酚基和吲哚基在一定條件下可解離;酸性胺基酸的側鏈都含有羧基;而鹼性胺基酸的側鏈分別含有氨基、胍基或咪唑基。
脯氨酸和半胱氨酸結構較為特殊。脯氨酸應屬亞胺基酸,N在雜環中移動的自由度受限制,但其亞氨基仍能與另一羧基形成肽鍵。脯氨酸在蛋白質合成加工時可被修飾成經脯氨酸;半胱氨酸巰基失去質子的傾向較其他胺基酸為大,其極性最強;2個半胱氨酸通過脫氫後以二硫鍵相連接,形成胱氨酸。蛋白質中有不少半胱氨酸以胱氨酸形式存在。
在蛋白質翻譯後的修飾過程中,脯氨酸和賴氨酸可分別被羥化為羥脯氨酸和羥賴氨酸。蛋白質分子中20種胺基酸殘基的某些基團還可被甲基化、甲醯化、乙醯化、異戊二烯化和磷酸化等。這些翻譯後修飾,可改變蛋白質的溶解度、穩定性、亞細胞定位和與其他細胞蛋白質相互作用的性質等,體現了蛋白質生物多樣性的一個方面。
胺基酸具有共同或特異的理化性質
[編輯]胺基酸具有兩性解離的性質
[編輯]由於所有胺基酸都含有鹼性的α-氨基和酸性的α-羧基,可在酸性溶液中與質子(H+)結合呈帶正電荷的陽離子 (—NH3+), 也可在鹼性溶液中與OH-結合,失去質子變成帶負電荷的陰離子(—COO-), 因此胺基酸是一種兩性電解質,具有兩性解離的特性。胺基酸的解離方式取決於其所處溶液的酸鹼度。在某一pH的溶液中,胺基酸解離成陽離子和陰離子的趨勢及程度相等,成為兼性離子,呈電中性,此時溶液的pH稱為該胺基酸的等電點(amino acid isoelectric point ,pI)。
通常胺基酸的等電點(pI)是由α-羧基和α-氨基的解離常數的負對數pK1和pK2決定的。
pI的計算公式為:pI=(pK1+pK2)。
如丙氨酸pK-COOH=2.34,pK-NH2=9.69,所以丙氨酸的pI=(2.34+9.69)=6.02。
若一個胺基酸有3個可解離基團,寫出它們電離式後取兼性離子兩邊的pK的平均值,即為此胺基酸的pl。
含共軛雙鍵的胺基酸具有紫外吸收性質
[編輯]根據胺基酸的吸收光譜,含共軛雙鍵的Trp和Tyr的最大吸收峰在280nm波長附近。由於大多數蛋白質含有Trp和Tyr殘基,因此測定蛋白質溶液280nm的光吸收值是分析溶液中蛋白質含量的快速簡便的方法。
胺基酸與茚三酮反應生成藍紫色化合物
[編輯]茚三酮反應(ninhydrin reaction)指的是茚三酮水合物在弱酸性溶液中與胺基酸共加熱時,胺基酸被氧化脫氨、脫羧,而茚三酮水合物被還原,其還原物可與胺基酸加熱分解產生的氨結合,再與另一分子茚三酮縮合成為藍紫色的化合物,此化合物最大吸收峰在570nm波長處。由於此吸收峰值的大小與胺基酸釋放出的氨量成正比,因此可作為胺基酸定量分析方法。
胺基酸通過肽鏈連接而形成蛋白質或肽
[編輯]蛋白質中的胺基酸相互結合而生成肽(peptide), 例如1分子甘氨酸的α-羧基和1分子甘氨酸的α-氨基脫去1分子水縮合成為甘氨醯甘氨酸,這是最簡單的肽,即二肽。α-羧基和α-氨基脫水形成醯胺鍵,稱為肽鍵。二肽通過肽鍵與另一分子胺基酸縮合生成三肽。此反應可繼續進行,依次生成四肽、五肽......
一般而言,由2~20個胺基酸相連而成的肽稱為寡肽(oligopeptide), 而更多的胺基酸相連而成的肽稱為多肽(polypeptide)。多肽鏈有兩端,其游離α-氨基的一端稱氨基末端(amino terminal)或N-端,游離α-羧基的一端稱為羧基末端(carboxyl terminal)或C-端。肽鏈中的胺基酸分子因脫水縮合而基團不全,被稱為胺基酸殘基(amino acid residue)。
蛋白質是由許多胺基酸殘基組成、摺疊成特定的空間結構、並具有特定生物學功能的多肽。一般而論,蛋白質的胺基酸殘基數通常在50個以上,50個胺基酸殘基以下則仍稱為多肽。例如,常把由39個胺基酸殘基組成的促腎上腺皮質激素稱作為多肽,而把含有51個胺基酸殘基、分子量為 5733的胰島素稱作蛋白質。
生物活性肽具有生理活性及多樣性
[編輯]人體內存在許多具有生物活性的低分子量的肽,有的僅三肽,有的屬寡肽或多肽,在代謝調節、神經傳導等方面起著重要的作用。隨著肽類藥物的發展,許多化學合成或重組DNA技術製備的肽類藥物和疫苗已在疾病預防和治療方面取得成效。
穀胱甘肽(GSH)
[編輯]
穀胱甘肽(glutathione, GSH)是由穀氨酸、半胱氨酸和甘氨酸組成的三肽。第一個肽鍵是非α肽鍵,由穀氨酸γ-羧基與半胱氨酸的氨基組成, 分子中半胱氨酸的巰基是該化合物的主要功能基團。
GSH的巰基具有還原性,可作為體內重要的還原劑保護蛋白質或酶分子中的巰基免遭氧化,使蛋白質或酶處在活性狀態。在穀胱甘肽過氧化物酶的催化下,GSH可還原細胞內產生的H2O2, 使其變成H2O, 與此同時,GSH被氧化成氧化型穀胱甘肽(GSSG), 後者在穀胱甘肽還原酶催化下,再生成GSH。
此外,GSH的巰基還有嗜核特性,能與外源的嗜電子毒物如致癌劑或藥物等結合,從而阻斷這些化合物與DNA、RNA或蛋白質結合,以保護機體免遭毒物損害。
多肽類激素及神經肽體
[編輯]內有許多激素屬寡肽或多肽,例如屬於下丘腦-垂體-腎上腺皮質軸的催產素(9肽)、加壓素(9肽)、促腎上腺皮質激素(39肽)、促甲狀腺素釋放激素(3肽)等。
促甲狀腺素釋放激素是一個特殊結構的三肽, 其N-端的穀氨酸環化成為焦穀氨酸(pyroglutamjc acid),C-端的脯氨酸殘基醯化成為脯氨醯胺,它由下丘腦分泌,可促進腺垂體分泌促甲狀腺素。
有一類在神經傳導過程中起信號轉導作用的肽類被稱為神經肽(neuro peptide)。較早發現的有腦啡肽(5肽)、β-內啡肽(31肽)和強啡肽(17肽)等。近年還發現孤啡肽(17肽),其一級結構類似於強啡肽。它們與中樞神經系統產生痛覺抑制有密切關係。因此很早就被用於臨床的鎮痛治療。除此以外,神經肽還包括P物質(10肽)、神經肽Y等。